
多くの病気は臓器内の細胞を破壊し、生命を奪ったり、通常の生活を送る能力を損ないます。たとえば、約 580 万人のアメリカ人が心不全を患っており、毎年 67 万人が心不全と診断されています 。心不全では、心筋自体の多くが壊死するため、心臓は血液を十分に送り出すことができなくなります。
同様に、約 2,360 万人のアメリカ人が糖尿病を患っています 。これらの人々の 5 ~ 10 パーセントは、膵臓のインスリン産生細胞が死滅した I 型糖尿病を患っています。最後に、約 100 万人のアメリカ人がパーキンソン病を抱えて暮らしています 。この病気では、運動の制御に役立つ神経伝達物質ドーパミンを作る細胞が死滅します。 パーキンソン病の患者には震えや制御不能な動きが見られます。しかし、これらの死んだ細胞を新鮮な細胞に置き換えることができたらどうなるでしょうか?患者たちは治療を受けて普通の生活を送ることができるでしょうか?それが幹細胞研究の目標です。
この記事では、上の添付画像から始めて について見ていきます。写真では、ES細胞のコロニーは、丸みを帯びた高密度の細胞の塊です。平らで細長い細胞は、「フィーダー細胞」として使用される線維芽細胞です。また、幹細胞がどのように機能するかを調べ、病気を治療する可能性を発見し、幹細胞の研究と使用をめぐる進行中の議論についても触れます。まずは、基本的なことをいくつか説明しましょう。
幹細胞の基礎
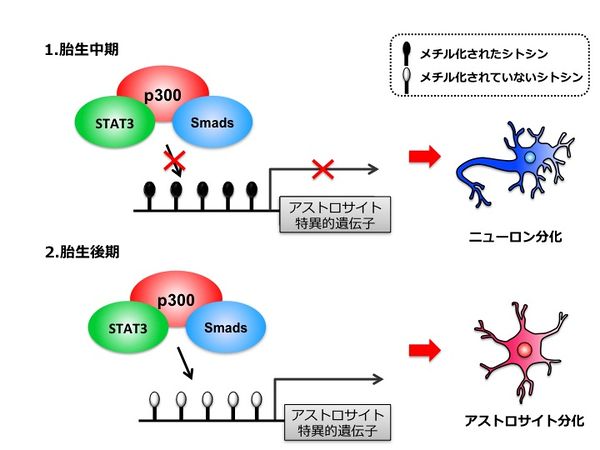
幹細胞は本質的に人体の構成要素です。幹細胞は長期間分裂することができ、特殊化されていませんが、特殊化された細胞に成長することができます。人体における最も初期の幹細胞は、ヒトの胎児に見られるものです。胚内の幹細胞は、最終的には胎児の体内のあらゆる細胞、組織、器官を生み出します。複製して独自の種類の細胞をさらに作り出すことしかできない通常の細胞とは異なり、幹細胞は多能性です。分裂すると、人体の220 個の異なる細胞のいずれかを作ることができます。幹細胞には自己複製能力もあり、何度も自己複製することができます。
幹細胞には次のようないくつかの種類があります。
- 胚性幹細胞– 胚性幹細胞には、胚、胎児、または臍帯血内に見られる細胞が含まれます。 ES細胞は、いつ採取されるかにもよりますが、人体のほぼあらゆる細胞を生み出すことができます。
- 成人幹細胞– 成人幹細胞は乳児、子供、成人に存在します。それらは、心臓、脳、腎臓などのすでに発達した組織に存在します。通常、それらは常在臓器内で細胞を生成します。
- 人工多能性幹細胞 (IPSC) – これらの幹細胞は、実験的に幹細胞様の状態に「再プログラム」された成体分化細胞です。
では、これらすべての種類の幹細胞はどのように機能するのでしょうか?そして、それらの潜在的な用途は何でしょうか?調べてみましょう — まずは胚性幹細胞から始めましょう。
胚性幹細胞
卵細胞が精子によって受精すると、分裂して胚になります。胎児の中には、人体のさまざまな種類の細胞のすべてになることができる幹細胞があります。研究のために、科学者は 2 つの方法で胚を入手します。多くのカップルは体外受精によって妊娠します。このプロセスでは、カップルの精子と卵子が培養皿内で受精します。卵子は胚に成長し、その後雌に移植されます。ただし、移植できる以上の胚が作られます。したがって、これらの胚は通常凍結されます。多くのカップルが未使用の胚を幹細胞研究のために寄付しています。
科学者が胚を取得する 2 番目の方法は、治療用クローン作成です。この技術は、(幹細胞治療を必要とする患者からの)細胞をドナー卵子と融合させます。卵子から核が取り出され、患者の細胞の核と置き換えられます。 (プロセスの詳細については、 「クローン作成のしくみ」を参照してください。)この卵子は、化学的または電気によって分裂するように刺激され、得られた胚は患者の遺伝物質を運ぶため、患者の体が幹を拒絶するリスクが大幅に軽減されます。移植された細胞。
既存の受精胚を使用する方法と、特に研究目的で新しい胚を作成する方法のどちらの方法も議論の余地があります。しかし、論争に入る前に、科学者が幹細胞を研究するために実験室環境で幹細胞を複製させる方法を見てみましょう。
胚に約 8 個の細胞が含まれる場合、幹細胞は全能性を持ち、あらゆる種類の細胞に成長することができます。 3 ~ 5 日で、胚は胚盤胞と呼ばれる細胞の球に成長します。胚盤胞には合計約 100 個の細胞が含まれており、その中に幹細胞があります。この段階では、幹細胞は多能性を持っており、ほぼあらゆる種類の細胞に成長することができます。

幹細胞を増殖させるために、科学者は幹細胞を胚盤胞から取り出し、研究室のペトリ皿で培養します(栄養豊富な溶液中で培養します)。幹細胞は数回分裂し、科学者は細胞集団を他の皿に分けます。数か月後には数百万の幹細胞が存在します。細胞が分化せずに増殖し続ける場合、科学者は幹細胞株を手に入れたことになります。細胞株を凍結して研究室間で共有することができます。後で説明するように、治療法の開発には幹細胞株が必要です。
今日、多くの妊婦が臍帯バンク、つまり出産後に臍帯血を保管するプロセスについて質問されます。なぜ誰かがそれをしたいのでしょうか?母親が出産すると、へその緒と残った血液は廃棄されることがよくあります。ただし、この血液には胎児の幹細胞も含まれています。臍帯血を採取し、胚性幹細胞を培養で増殖させることができます。発生初期の胚性幹細胞とは異なり、臍帯血由来の胎児幹細胞は多分化能があり、限られた数の細胞型に成長することができます。
ES細胞についての理解が深まったところで、成体幹細胞を見てみましょう。
成人幹細胞
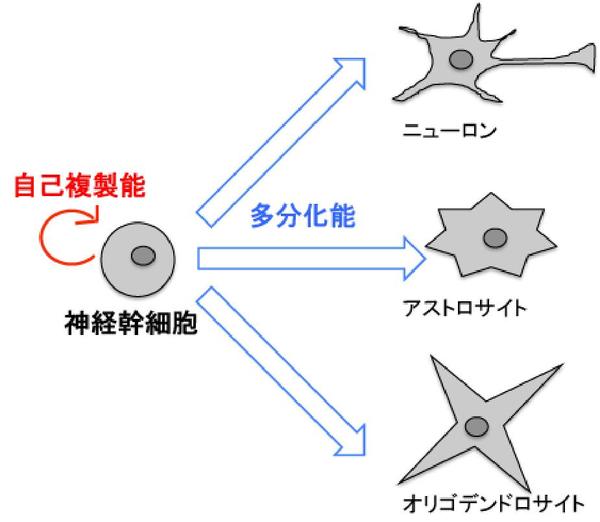
成体幹細胞は、病気、怪我、日常の磨耗によって損傷した細胞を再生する、私たちに組み込まれた修復キットと考えることができます。これらの未分化細胞は、組織または器官内の他の分化細胞の中に存在します。それらは分裂し、周囲の分化した細胞を修復または置換するように特殊化します。成体幹細胞の一般的な例は、赤色骨髄に存在する造血幹細胞です。これらの幹細胞はさまざまな血液細胞 (赤血球、リンパ球、血小板 – 詳細については「血液の仕組み」を参照) に分化します。たとえば、赤血球は再生することができず、約 28 日間生存できません。使い古された赤血球を置き換えるために、骨髄内の造血幹細胞が分裂して新しい赤血球に分化します。
骨髄には、間質幹細胞または間葉幹細胞として知られる 2 番目のタイプの成体幹細胞も含まれています。間質幹細胞は、骨、軟骨、脂肪、および骨に含まれる結合組織になります。成体幹細胞は、脳、骨格筋、血管、皮膚、肝臓、歯、心臓などの他の多くの組織でも見つかっています。ソースに関係なく、成体幹細胞は多分化能を持っており、限られた数の細胞型に成長することができます。
成体幹細胞は多くの組織に存在しますが、その数は少なく、おそらく周囲の細胞 100,000 個につき 1 個の成体幹細胞です。これらの幹細胞は周囲の細胞と似ているため、区別するのは困難です。しかし研究者は、「光を当てる」ことでそれらを識別する興味深い方法を開発しました。すべての細胞は、その表面に受容体と呼ばれる固有のタンパク質を持っています。受容体は、細胞間コミュニケーションの一環として、他の細胞からの化学メッセージに結合します。研究者は、これらの受容体、またはマーカーを使用して、幹細胞上の特定の受容体に結合する化学メッセージを蛍光分子で「タグ付け」することにより、成体幹細胞を識別および単離します。蛍光化学メッセージが幹細胞の表面の受容体に結合すると、幹細胞は蛍光の下で「光ります」。その後、「光った」幹細胞を識別し、単離することができます。
胚性幹細胞と同様に、成体幹細胞も培養で増殖させて幹細胞株を確立できます。
かつて、成体幹細胞は胚性幹細胞よりも限定されており、その起源と同じ種類の組織しか生じないと考えられていました。しかし、新しい研究では、成体幹細胞には他の種類の細胞も生成する可能性があることが示唆されています。たとえば、肝細胞は、通常は膵臓によって生成されるインスリンを生成するように誘導される可能性があります。この能力は可塑性または分化転換として知られています
幹細胞には胚細胞と成体細胞の 2 種類しかないと考えられていましたが、幹細胞ブロックにはもう 1 種類の細胞が存在します。この「新しい」タイプ、人工多能性幹細胞について学ぶために読み続けてください。
人工多能性幹細胞 (IPSC)
胚であろうと成体組織であろうと、幹細胞はほとんどありません。しかし、多くは細胞治療に必要です。 ES細胞の使用には倫理的および政治的な問題があったため、成人からより多くの幹細胞を入手する方法があれば、論争は少なくなるかもしれない。 IPSCに入ります。
体内のすべての細胞には同じ遺伝的指示があります。それでは、心臓細胞は肝臓細胞と何が違うのでしょうか? 2 つの細胞は異なる遺伝子セットを発現します。同様に、幹細胞は特定の遺伝子セットをオンにして別の細胞に分化します。では、分化した細胞を再プログラムして幹細胞に戻すことは可能でしょうか? 2006 年、科学者たちはまさにそれを行いました。彼らはウイルスを使用して、4つの幹細胞因子を皮膚細胞に送り込みました。これらの要因により、分化した幹細胞は胚性幹細胞のような状態になりました。得られた細胞は人工多能性幹細胞(IPSC)と呼ばれ、ヒト胚性幹細胞と多くの特徴を共有しました。 IPSC の構造は類似しており、同じマーカーと遺伝子を発現し、同じように増殖しました。そして研究者らは、IPSC を細胞株に増殖させることができました。
人体には、胚性または成人の幹細胞よりも多くの分化した細胞が存在します。したがって、皮膚細胞のような患者自身の分化した細胞から膨大な量の幹細胞を作製できる可能性がある。 IPSC の作製には胚が関与しないため、幹細胞研究に関わる倫理的および政治的問題を回避できます。ただし、ISPSC の作成は最近の開発であるため、科学者は ISPSC を治療に使用する前にさらに研究を行う必要があります。まず、「再プログラミング」プロセスをよりよく理解する必要があります。そして、IPSC が胚性幹細胞と十分に類似しているのか、それとも実際に同一であるのかを調査する必要があります。現在の研究はこれらの問題に焦点を当てていますが、細胞を再プログラミングして IPSC を作製することには大きな可能性があります。
幹細胞とは何か、そしてその働きについてはよく理解できたので、次に幹細胞を病気の治療にどのように使用できるかを見てみましょう。
歯科医は通常、親知らずを抜いた後は廃棄しますが、保存し始めるべきかもしれません。それらは幹細胞を作るのに役立つかもしれません。最近、日本の科学者のグループが、抜歯した親知らずの歯髄から人工多能性幹細胞(IPSC)を作製した。彼らはウイルスを使用して、第三大臼歯の歯髄から単離された間葉系間質細胞に幹細胞因子を送達した。得られた IPSC は胚性幹細胞に類似していました。
2003年、NIHの研究者サンタオ・シーは娘の乳歯から幹細胞を抽出した。幹細胞は培養で増殖し、マウスに移植すると骨を形成する可能性がある。潜在的には、将来の使用のために歯から幹細胞を保存できるかもしれませんが、それは高価なプロセスになるでしょう。
もしかしたら、歯の妖精がその歯を使ってやっているのかもしれない?
幹細胞を使った病気の治療
病気の治療に幹細胞を使用する最初のステップは幹細胞株を樹立することであり、研究者たちはこれを達成しました。次に、科学者は、幹細胞が望む任意の細胞に分化できるように、幹細胞内の特定の遺伝子をオンにすることができなければなりません。しかし、科学者たちはまだこれを行う方法を学んでいません。そのため、幹細胞の分化の研究は活発な研究分野です。科学者が幹細胞から分化した細胞を作成できれば、薬物検査や細胞ベースの治療など、その利用の可能性が数多く広がります。たとえば、心臓病を治療するための新薬をテストしたいとします。現在、新薬は動物で試験する必要があります。動物研究からのデータは、ヒトでの臨床試験の前に解釈され、ヒトに推定される必要があります。しかし、人間の心臓細胞で直接テストできると仮定してみましょう。これを行うには、培養皿内でヒト幹細胞株を処理してヒト心臓細胞に分化させることが考えられます。潜在的な薬剤をそれらの細胞でテストでき、そのデータは人間に直接適用できるでしょう。この使用により、新薬を市場に出す際に膨大な時間と費用を節約できる可能性があります。
幹細胞ベースの治療は新しいものではありません。最初の幹細胞ベースの治療法は、白血病の治療に使用される骨髄移植でした。この処置では、患者の既存の骨髄が放射線および/または化学療法によって破壊されます。ドナーの骨髄が患者に注入され、骨髄幹細胞が患者の骨に定着します。ドナーの骨髄細胞は、患者が必要とする血液細胞に分化します。多くの場合、患者は免疫系が新しい骨髄を拒絶するのを防ぐために薬を服用しなければなりません。しかし、この手順では既存の造血幹細胞が使用されます。幹細胞株をどのように使用しますか?幹細胞が心不全の治療にどのように使用されるかを見てみましょう。
理想的には、機能不全の心臓を治療するために、科学者は幹細胞を刺激して心臓細胞に分化し、それを患者の損傷した心臓に注入することができます。そこでは新しい心臓細胞が成長し、損傷した組織を修復することができます。科学者たちはまだ幹細胞を心臓細胞に分化させることはできていないが、この考えをマウスで実験した。彼らは、心臓に損傷を負ったマウスに幹細胞(成体、胎児)を注入しました。細胞は損傷した心臓細胞内で増殖し、マウスの心臓機能と血流の改善が見られました。
これらの実験において、幹細胞が心臓機能をどのように改善したかについては、依然として議論の余地がある。それらは新しい筋肉細胞を直接再生した可能性があります。あるいは、損傷領域への新しい血管の形成を刺激した可能性もあります。そして、新しい血流が既存の心臓幹細胞を刺激して、新しい心筋細胞に分化させた可能性があります。これらの実験は現在評価中です。
幹細胞の使用における大きな障害の 1 つは、拒絶反応の問題です。提供された胚から採取した幹細胞を患者に注射すると、患者の免疫系が細胞を外来侵入者とみなして攻撃を開始する可能性があります。成人幹細胞または IPSC を使用すると、患者から採取された幹細胞が免疫系によって拒否されないため、この問題をある程度克服できる可能性があります。しかし、成体幹細胞は胚性幹細胞よりも柔軟性が低く、研究室で操作するのが困難です。また、IPSC 技術は移植作業には新しすぎます。
最後に、幹細胞が特殊な細胞にどのように分化するかを研究することで、得られた情報を利用して、先天異常がどのように発生するのか、場合によってはその治療方法を理解することができます。
では、幹細胞研究にこれほどの可能性があるのであれば、なぜ論争が起こるのでしょうか?現在の倫理的および政治的問題を調査してみましょう。
幹細胞研究の論争
幹細胞研究は、世界中の科学界と宗教界を二分する最大の問題の 1 つとなっています。この問題の核心にあるのは、「人生はいつ始まるのか?」という 1 つの中心的な質問です。現時点では、信頼できる幹細胞を入手するには、科学者はすでに妊娠した胚を使用するか、患者の体からの細胞と提供された卵子を使用して胚のクローンを作成する必要があります。いずれにせよ、胚の幹細胞を採取するには、科学者はそれを破壊する必要があります。その胚には4つか5つの細胞しか含まれていないかもしれないが、一部の宗教指導者は、それを破壊することは人間の命を奪うことと同じだと言う。必然的に、この問題は政治の場にも持ち込まれました。
1996 年、議会はディッキー・ウィッカー修正案と呼ばれる連邦歳出法案の特約を可決しました。ジェイ・ディッキー下院議員とロジャー・ウィッカー下院議員は、ヒトの胚を作成または破壊する研究への連邦資金の使用を禁止することを提案した。幹細胞研究の主な資金源は連邦政府の資金です。それ以来、この改正は毎年更新されています。
2001 年、ジョージ W. ブッシュ大統領は連邦政府による幹細胞研究をさらに制限しました。ブッシュ大統領は大統領令の中で、連邦資金はすでに樹立されたヒト胚性幹細胞株(22細胞株のみ)の研究にのみ使用できると述べた。このため、研究者は研究用にさらに多くの胚性幹細胞株を作成することができなくなりました。
2009年、バラク・オバマ大統領は、ES細胞の研究を拡大する大統領令を出した。オバマ政権は、以下の条件が適用される場合、胚性幹細胞研究に対する連邦政府の資金提供を許可しました。
- この細胞株はブッシュ政権時代に存在していた22株のうちの1株か、体外受精後に廃棄された胚から作られたものだった。
- 胚の提供者にはいかなる形でも報酬は支払われなかった。
- ドナーは、同意する前に、胚が研究目的で使用されることを明らかに知っていました。
同政権によると、その資金は新しい胚の作成(すでに民間の手段で作成されていた)に資金を提供したものではなく、それらの破壊にも資金を提供しなかったため、新しい政策はディッキー・ウィッカー修正条項に違反しなかった。
2009年、ボストンの2人の研究者、ボストン生物医学研究所のジェームス・シャーリー博士とアバ・マリア・バイオテクノロジー・カンパニーのテレサ・ダイッシャー博士およびその他の機関が政府を相手取って訴訟を起こした。当初、裁判官が原告には法的立場がない(つまり、原告は新しい規則によって実質的な影響を受けていない)との判決を下したため、訴訟は却下された。しかし、控訴裁判所は最初の判決を覆しました。 2人の科学者は引き続き原告となった。科学者らは、研究では成体幹細胞のみを使用しているため、新しい規則により連邦研究費の獲得競争が激化し、資金獲得に影響を与えると主張した。ロイス・ランバース連邦判事は控訴裁判所の判決を支持した。彼は新しい規則の施行を阻止する差し止め命令を出した。同氏は、胚性幹細胞株を作成する過程で胚を破壊しなければならないため、この規則はディッキー・ウィッカー修正条項に違反していると主張した。
2010年9月、ニューヨーク・タイムズは、米国控訴裁判所がランバース判事の判決を検討している間、新規則の下でも胚性幹細胞研究への連邦政府の資金提供は継続できるとの判決を下したと報じた。この判決により、この裁判所が判決を下すか、米国最高裁判所が検討するか、あるいは議会が問題を明確にする法案を可決するまで、研究者は胚性幹細胞培養物を与えたり、マウスで実験したり、その他の研究活動を続けることが認められる。その一方で、幹細胞研究と幹細胞研究者のキャリアは法的なジェットコースターのような状況にあります。幹細胞には病気を治療する大きな可能性がありますが、科学、倫理、法律の面では多くの研究が残されています。
幹細胞の詳細については、次のページのリンクを調べてください。
俳優のマイケル・J・フォックスは、パーキンソン病(運動に影響を及ぼす脳の変性疾患)と診断された1991年以来、幹細胞研究を声高に主張してきた。彼の財団は、パーキンソン病の研究に資金を提供するために 2 億 500 万ドル以上を寄付しました 。フォックスとその財団は、いつか科学者が幹細胞を誘導して、パーキンソン病患者には体内で欠乏している化学物質であるドーパミンを生成させることができるようになるのではないかと期待している。
ナンシー・レーガン元大統領夫人も、夫のロナルド・レーガン元大統領が別の脳変性疾患であるアルツハイマー病に罹患した際に、幹細胞研究の提唱者となった。彼は 2004 年の夏にアルツハイマー病で亡くなりました。